多靶点描绘复杂的肿瘤微环境对于全面评估患者的预后和接受免疫抑制剂治疗的疗效,挖掘肿瘤微环境与肿瘤发生发展、复发、转移和耐药机制的关系和临床分子机理提供了全新的思路,依托下一代病理技术(NGP),即多重荧光免疫组化技术平台,阔然基因推出了肿瘤免疫微环境全景分析解决方案,助力于更精确的肿瘤免疫和其他药物开发应用。
本期NGP资讯,将为大家分享两篇NGP在肺癌研究中的应用案例。
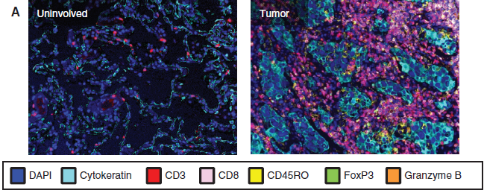
肿瘤浸润性T淋巴细胞(TIL)在癌症生物学中有重要作用,但TIL表型与其对局部非小细胞肺癌 (NSCLC) 的预后相关性之间的关系尚不明确。
研究者入组了150名局部NSCLC患者的新鲜肿瘤和正常邻近组织。通过NGS、高维流式细胞术和多重荧光免疫组化(mIHC)等技术全面表征组织微环境,结果表明:TIL的浸润程度与局部NSCLC无显著的预后关系;实验数据确定了两种主要的免疫类型(IM1和IM2),可预测独立于临床特征的无复发生存期;IM2与不良预后相关,IM1与良好的预后相关;预后良好的亚组与缺乏抑制性受体的T细胞和存在三级淋巴结构有关。
该研究确定了NSCLC中两种主要的预后相关免疫类型,独立于患者的肿瘤特征和临床特征,值得在未来的研究中进行探索。
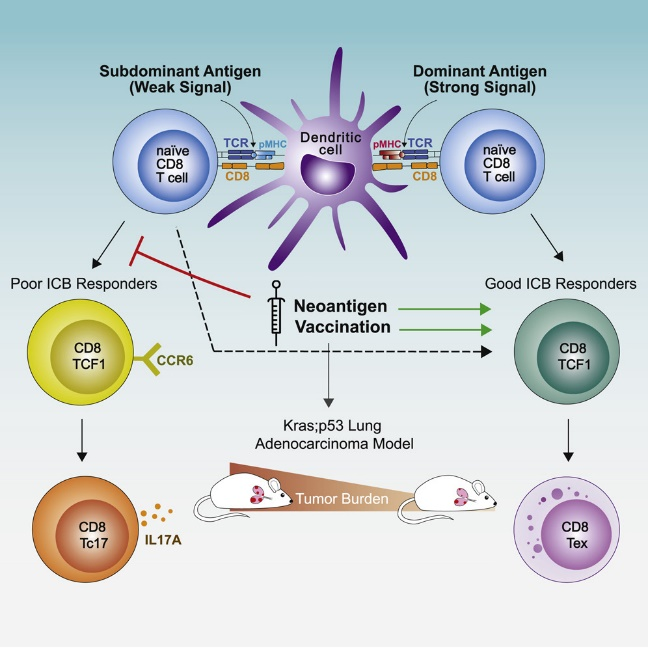
CD8+ T细胞对不同肿瘤新抗原的反应是同时发生的,但对反应之间的相互作用及其对 T 细胞功能和肿瘤控制的影响尚不明确。
为了研究T细胞对肿瘤的免疫过程及其和肿瘤新抗原的相互关系,研究者通过单细胞测序技术和多重荧光免疫组化技术(mIHC),在小鼠肺腺癌中发现:肿瘤中建立了免疫优势,CD8+ T细胞的扩张主要由最稳定结合MHC的抗原驱动;响应亚显性抗原的CD8+ T细胞富含了与免疫检查点阻断(ICB)反应相关的TCF1+ 祖细胞。CCR6+ TCF1+ 祖细胞对ICB反应的贡献很小;接种疫苗可消除CCR6+ TCF1+ 祖细胞并改善亚显性反应。
该研究表明通过免疫调节T细胞组细胞亚群,优化T细胞对亚优势新抗原的反应,可以获得更好的ICB反应。
目前,阔然基因已经布局了整套多重荧光免疫组化技术(mIHC)平台,包括Kreep染色试剂盒、KR-HT5高通量荧光病理切片扫描系统和KRIAS医学病理影像分析软件,并开发了6款检测产品。
三大技术突破

依托多重荧光免疫组化技术平台,阔然基因推出了肿瘤免疫微环境全景分析解决方案,全景剖析肿瘤免疫微环境中的杀伤性T细胞、耗竭性T细胞、巨噬细胞、B细胞、三级淋巴结构和免疫检查点受体的浸润情况,全面评估患者的预后和接受免疫抑制剂治疗的疗效,挖掘肿瘤免疫微环境与肿瘤发生发展、复发、转移和耐药机制的关系和临床分子机理。
参考文献:
[1] Ann Oncol.2022 Jan;33(1):42-56.
[2] Cell.2021, 16; 184(19): 4996-5014

